La Chimiluminescence
La chimiluminescence est une réaction chimique produisant de la lumière, dont lune des plus connues est la réaction du luminol. Le phénomène de Chimiluminescence est facile à observer lors de loxydation lente du phosphore dans lair, il se dégage alors une faible luminescence verte, cest le principe du feu follet, lueur pâle, jaune, verte, bleu ou rouge pouvant être aperçue près des marais et dans les cimetières. Le feu follet est dût à loxydation du méthane et de la phosphine issus de la décomposition de matières organiques.
Le phosphore
De symbole P et de numéro atomique 15, le phosphore est dit « blanc » à létat pur, alors quil arbore une couleur légèrement ambrée. Son nom vient du mot grec fosforos signifiant « porteur de lumière » car le phosphore émet une faible lueur dans lobscurité alors quil est exposé à lair.

Phosphore blanc en poudre.
Le phosphore est indispensable à la vie, cest un constituant des os et du système nerveux, il est aussi essentiel dans la formation dacides nucléiques (ADN et ARN), il est, dans ce cas, toujours accompagné de 4 atomes doxygènes (PO4) cest aussi le onzième élément le plus présent dans la croute terrestre (0.12%), ainsi qu'un élément aux variétés allotropiques, c'est-à-dire quà létat solide, il existe sous plusieurs formes (Poudre, cristal ), dans le cas du phosphore, il existe le phosphore blanc, rouge et noir. Le phosphore rouge, moins inflammable et moins toxique que le phosphore blanc, a été adopté dans les allumettes, il sobtient par chauffage à 200°C. Le phosphore noir, lui, a ses atomes rangés à la manière du graphite, c'est-à-dire en couches hexagonales et est obtenu par fort chauffage du phosphore blanc, et à haute pression pour quil soit sous sa forme la plus stable.
Minéraux
De nombreux minéraux sont phosphorescents. Toutefois, pour être aisément vu, il faut que l'intensité lumineuse ou la durée soit suffisante. Certains gardent ainsi leur luminosité pendant plusieurs jours.
La phosphorescence peut aussi être produit par la présence dans le minéral d'éléments étrangers, souvent en très petite quantité. Ces éléments sont appelés "activateurs". D'autres éléments, comme le fer ou le cobalt, peuvent aussi empêcher la phosphorescence même si un activateur est présent. Ils peuvent être appelés "désactivateurs".
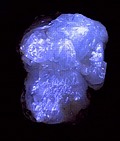
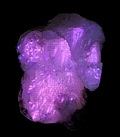
La calcite de Terlingua (Texas) phototographiée
 |
 |
 |
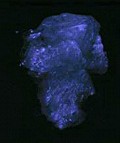 |
| en lumière du jour | sous ondes longues | sous ondes courtes | après avoir éteint les ondes courtes. forte phosphorescence |
La natrolite
Cristaux allongés en agrégats fibreux de teinte grisâtre.
 |
| lumière naturelle |
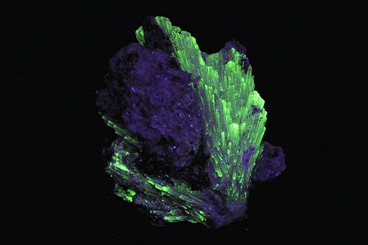 |
| NATROLITE Mont Saint-Hilaire, Québec, CANADA L 3 x H 4 x P 3,5 cm |
| UV courts |
| collection et photographie © Patrick Arweiler |
La willemite
 |
 |
seule fois dans une petite cavité. La phosphorescence est aussi très forte et ressemble à la fluorescence en UV court. |
La fluorine
La fluorine est un assemblage d'ions Ca2+ et F-. Les anions F- sont deux fois plus nombreux que les cations Ca2+.
La structure de la fluorine correspond à un remplissage d'une structure hôte.
Les anions F- forment un réseau cubique simple dans lequel les cations Ca2+ occupent la moitié des sites cubiques. Les cations et les anions ont à peu près la même taille. Il est aussi possible d'inverser les rôles des cations et des anions et de considérer que les cations Ca2+ forment un réseau hôte cubique à faces centrées et les anions F- occupent tous les sites tétraédriques. Ces deux visions sont équivalentes.
 |
 |

